بخشی از پاورپوینت
--- پاورپوینت شامل تصاویر میباشد ----
اسلاید 1 :
مقدمه
پيل سوختي يک وسيله الکتروشيميايي است که انرژي شيميايي را به انرژي الکتريکي تبديل مي کند و از الكتروليت، الكترود آند و الكترود كاتد تشكيل شده است.
اسلاید 2 :
تاريخچه
- 1820ميلادي: ساخت پيل سوختي بسيار ساده توسط سر هامفري امکان توليد شوک الکتريکي بسيار ساده اي
- 1839ميلادي: تحقيق در مورد روش اتصال سري - موازي کردن باطري روي پلاتينيوم توسط سر ويليام گرو
- آزمايش توليد اکسيژن و هيدروژن از الکتروليز آب
- مشاهده: اگر جريان منبع تغذيه قطع گردد جريان کوچک ولي قابل اندازه گيري در جهت مخالف جاري ميشود.
پديده پيل سوختي
اسلاید 3 :
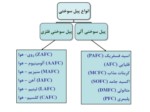
تاريخچه انواع پيلهاي سوختي
- پيلسوختي اسيد فسفريك:
1842 ميلادي: استفاده از اسيد به عنوان الکتروليت توسط گرو
توجه: اسيد فسفريک يک رساناي ضعيف الکتريسيته بود و جذاب نبود، بنابراين نسبت به انواع پيلسوختي آهستهتر توسعه يافتند.
- پيلسوختي قليايي:
1930 ميلادي: جايگزيني هيدروکسيدپتاسيم الکتروليت با اسيدسولفوريك توسط فرانسيس بيکن
توجه: هيدروکسيدپتاسيم کارايي مشابه اسيد سولفوريك را دارد ولي خورنده الکترودها نمي باشد.
اسلاید 4 :
تاريخچه انواع پيلهاي سوختي (ادامه)
- پيلسوختي اکسيد جامد:
1965 ميلادي: توليد اولين سري پيلسوختي اكسيد جامد توسط آرچر
توجه: توان پيل 100 وات و الكتروليت آن زيركونياي پايدار شده توسط كلسيم و الكترودها از جنس پلاتين
- پيلسوختي متانولي:
1995 ميلادي: جديدترين فنآوري پيلسوختي در دهه اخير
اسلاید 5 :
اجزاي پيل سوختي و وظايف آنها
- آند (الکترود سوخت):اکسيداسيون سوخت
- ايجاد سطح مشترک براي سوخت و محلول الکتروليت
- هدايت الکترونها از محل واکنش به سمت مدار خارجي
- کاتد (الکترود اکسيژن): احياء اکسيژن
- ايجاد سطح مشترک براي اکسيژن و الکتروليت
- هدايت الکترونها را از مدار خارجي به سمت کاتد
- الکتروليت
- انتقال يکي از انواع يونهاي ايجاد شده در واکنش الکترودها
- جلوگيري از عبور الکترونها
- وظيفه جداسازي گاز
اسلاید 6 :
نحوه عملکرد پيل سوختي
- هيدروژن به سمت آند هدايت مي شود و با از دست دادن الکترون به پروتون تبديل مي شود.
- در کاتد هوا دميده مي شود تا اکسيژن مورد نياز مهيا شود.
- اکسيژن الکترونها را از کاتد مي گيرد و به يون تبديل ميشود و در الکتروليت باقي مي ماند.
- ماده سراميکي بکار رفته به يونهاي اکسيژن اجازه مي دهد تا از ميان آن عبور کنند.
- پروتون با يون اکسيژن ترکيب مي شود و آب توليد مي کند و از طرف آند خارج مي شوند.
- الکترونهاي توليد شده در اين واکنش اکسايش-کاهش باعث ايجاديک اختلاف پتانسيل در دو سر پيل مي شوند. (مدار خارجي)
اسلاید 7 :
پيل سوختي اسيد فسفريک
- الکتروليت: با غلظتي در حدود %100
- محدوده دماي كاركرد: بين 150 تا 220 درجه سانتيگراد
- كاتاليست: پلاتين
- ماتريس نگهداري اسيد:
كاربيد سيليكون
- توان: 200 کيلووات
- آزمايش:
در واحدهايي با توان 11 مگاوات
- بازده الكتريكي: 45%-40%
اسلاید 8 :
پيل سوختي قليايي
- غلظت الكتروليت هيدروكسيد پتاسيم با دما تغيير ميکند.
- محدوده دماي عملياتي: از 150 تا 220 درجه سانتيگراد
- يك ماتريس متخلخل (از جنس آزبست) جهت نگهداري الكتروليت که محلول برپايه آب است.
- الكتروكاتاليست:
نيكل، نقره و اكسيدهاي فلزات
- بازده: درحدود %70
- طول عمر: بيش از 10000 ساعت
- حساسيت زياد به CO2
- ارزاني کاتاليست
اسلاید 9 :
پيل سوختي کربنات مذاب
- الكتروليت: تركيبي ازكربنات مذاب نمكها درماتريسي از جنس LiAlO2
- دو نوع ترکيب پرکاربرد: ترکيب كربنات سديم و کربنات ليتيم و يا کربنات پتاسيم وکربنات ليتيم
- دماي كاركرد:
600 تا 700 درجه سانتيگراد
- آند: نيكل كاتد: اكسيد نيكل
- بازده: حدود %60 درصد
- حساسيت كمتر نسبت به مسموميت CO
- پيچيدگي كار با الكتروليت مايع
- نياز به تزريق CO2در كاتد براي جبران يونهاي كربنات الكتروليت مصرف شده در واكنشهاي آند
اسلاید 10 :
پيل سوختي اکسيد جامد
- الكتروليت جامد سراميكي نازك به جاي الكتروليت مايع
- محدوده دماي عملكرد:
600 -1000 درجه سانتيگراد
- دو ساختار صفحه اي و لولهاي
- طول عمر: بيش از 40000 ساعت
- تنوع در سوخت مورد استفاده
- امکان تبديل مستقيم سوخت هيدروکربني بدون نياز به مبدل سوخت
- راندمان بالا 60-45 درصد، در ترکيب با يک توربين 70%
- امکان بکارگيري در مولدهاي توامان برق و حرارت