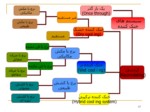
بخشی از پاورپوینت
اسلاید 1 :
ماهیت یک ماده شیمیایی بستگی به نوع ،تعداد وآرایش اتمهای تشکیل دهندهآن ماده دارد ودر صورت وقوع واکنش شیمیایی مواد به مواد جدیدی تبدیل می شوند اغلب برای شروع واکنش شیمیایی ابتد مواد اولیه با هم در تماس قرار می گیرند پس با شکسته شدن پیوندهای موجود بین این مواد و تشکیل پیوند های جدید , محصولات تولید می شوند.
اگر از تبدیل ماده Aمحصول Bتولید شود و امکان تبدیل ماده B به Aنباشد این واکنش رابرگشت ناپذیر گویند. حال واکنشی را در نظر بگیرید که مادهAبهBتبدیل می شود و طبق اصل لو شا تلیه با افزایش غلظت B , علاوه بر تبدیل ماده Aبه Bامکان تبدیل ماده BبهAنیز وجود دارد این واکنش را تعادلی گویند زیرا بعد از مدتی سرعت تبدیل A به B با سرعت تبدیل Bبه Aبرابر و شرایط تعادلی در سیستم برقرار شود .
به طور کلی واکنش ها را می توان به هفت دسته احتراق, سنتز ,تجزیه , جانشینی یگانه جانشینی متقابل , اسید _ باز و پلیمری طبقه بندی کرد.
n
اسلاید 2 :
nاحتراق
احتراق(COMBUSTION) این واکنش ترکیب اکسیژن با مواد کربن دار است. محصولات اصلی این واکنش آب, دی اکسید کربن می باشد. در طول این واکنش مقدار زیادی گرما آزاد می شود واکنشهایی که در کوره های صنعتی برای ایجاد حرارت صورت می گیرد نیز از این نوع است.
- سنتز
سنتز (SYNTHESIS)سنتز به واکنشی اطلاق می شود که طی آن دو یا چند ماده باهم ترکیب شده و یک ماده جدید را ایجاد می کنند.
nتجزیه
تجزیه(DECOMPOSITION) این واکنش عکس سنتز است که در آن یک مو لکول پیچیده به دو یا چند مولکول ساده تر تجزیه می شوند.
اسلاید 3 :
nجانشینی یگانه
در این واکنش یک جز از یک ماده با یک جز از یک دیگر مبادله می شوند .از این نوع واکنش می توان به واکنش منیزیم با آب اشاره کرد.
nجانشینی متقابل
این واکنش و قتی اتفاق می افتد که دو جز از دو ماده مختلف جای خود را با هم عوض کنندو دو ماده با خواص جدید ایجاد شود.
nاسید و باز
این واکنش یکی از انواع واکنش های جانشینی متقابل است که بین یک اسید وباز اتفاق می افتد که به تولید آب و نمک می انجامد.
اسلاید 4 :
n
واکنش شیمیایی عبارت است از تشکیل پیوند بین اتمها , شکسته شدن پیوند مولکولها و تشکیل پیوندهای جدید بین اتمها برای ایجاد محصولاتی با خواص جدید و متفاوت با خواص ماده اولیه. دریک واکنش شیمیایی ماده AباBوارد واکنش شده و بعضی از پیوندهای بین مولکولی هر دو ماده باز می شوند. مواد آزاد شده این پیوندها تمایل به تشکیل پیوندهای جدید ودر نتیجه مواد جدید و متفاوت با مواد AوB ایجاد می شوند.
A+B C+D
n
ماده AوBواکنشگر DوC محصول واکنش هستند.
n
n
n
اسلاید 5 :
یک از عوامل مهم در انجام واکنش ,تعداد برخورد ها بین مواد واکنش گر است. هر چه برخورد
بیشتر باشد احتمال انجام واکنش و تبدیل مواد واکنشگر به محصولات بیشتر می شود.
انجام واکنش فقط هنگامی امکان پذیر است که مولکولها با هم برخورد موثر نمایند و ایجاد برخورد بین مولکولها نیازمند انرژی است. حداقل انرژی لازم برای اینکه واکنشگرها در شرایط واکنش قرار بگیرند یا به عبارتی حداقل انرژی لازم برای شروع واکنش , انرژی اکتیواسیون نامیده شود . این میزان انرژی برای واکنشهای مختلف متفاوت است. علاوه بر انرژی , پارامترهایی چون نظریه بر خورد بین مولکول ها نیز در انجام واکنش موثر است. به همین
دلیل برخورد هایی که منجربه انجام واکنش می گردد,برخوردهای موثر نامیده می شوند.
پس از انجام برخوردهای موثر ورسیدن واکنشگرها به انرژی اکتیواسیون خود ,مقداری از مواد اولیه به محصول تبدیل می شود . برای بررسی میزان تبدیل مواد اولیه به محصول از درصد تبدیل استفاده می شود. درصد تبدیل عبا رت است از میزان محصولات تولید شده به میزان محصولات اولیه ,هر چه تعداد بر خورد های موثر بیشتر باشد درصد تبدیل پایین تر است. تعداد برخوردهای بیشتر به میزان مواد اولیه ورودی وابسته است .
برای تعیین میزان مواد در ظرف واکنش از پارامتری به نام غلظت استفاده می شود .
اسلاید 6 :
میزان جرم موجود از یک ماده در واحد حجم را غلظت می نامند. در مواردیکه در محیط واکنش گاز داشته باشیم برای اندازه گیری غلظت از فشار استفاده می کنیم. فشار ظرف واکنش برابر مجموع فشار اجزایی است که در ظرف واکنش موجود است به فشار هر کدام از اجزا فشار جزیی آن ماده می گو یند.
که بیانگر غلظت آن جز است. یکی دیگر از پارامترهای موثر برای انجام واکنش انرژی است که این انرژی خودتابعی از دماست گاهی برای کاهش میزان انرژی اکتیواسیون واکنش از کاتالیست استفاده می شود . کاتالیست ماده ی است که منجربه کاهش انرژی اکتیواسیون شده و به طور عملی پس از انجام واکنش بدون تغییر باقی می ماند.زمان واکنش در حضور کاتالیست کوتاهتراست .نکته مهم در مورد کاتالیست اینست که اگر امکان واکنش دوماده وجودنداشته باشد کا تالیست روی این ماده بی تاثیر است. کاتا لیستا عمر مفیدی دارند که بعداز پایان این زمان کارایی خود را از دست داد, و نیاز است که آنها را به نحوی فعال کنیم. این عمل را احیاء کاتالیست می گویند و برای این کار از فرآیند احیاء استفاده می کنند. شرایط مطلوب در یک واکنش این است که سرعت واکنش را بالا ببریم تا در زمان کوتاه بازده بالایی داشته باشیم یا این که سرعت واکنش را برای برخی واکنش های مفید کاهش داده یا متوقف سازیم . واکنش ساده تبدیل AبهB را در نظر بگیرید ساده ترین رابطه ریاضی که برای سرعت واکنش ارائه
اسلاید 7 :
می شود به صورت K.Cn A = سرعت واکنش
است , که در آن Kثابت سرعت واکنش بوده و تابعی از دماست . n درجه واکنش و CAبیانگر غلظت جزیA در مخلوط واکنش می باشد . گاهی محیط واکنش فقط مایع ,گاز یا جامد است وگاهی مخلوطی از این سه فاز اگر واکنش فقط در یک فاز انجام شود به آن همگن گویند . در یک واکنش همگن همه واکنشگرها ,محصولات و مواد شیمیایی در یک فاز هستند اگر در محیط حداقل دو فاز موجود باشند ,واکنش را غیر همگن یا نامتجانس گویند.
برخی واکنشهای شیمیایی با آزادکردن انرژی همراه هستند.این انرژی می تواند بصورت گرما به نور یا صدا باشد. چنین واکنشهایی را واکنش گرمازا گویند. بعضی دیگر از واکنشها گرماگیرند
یعنی برای انجام واکنش نیاز به انرژی داریم,به همین دلیل این واکنشها به طور معمو ل به صورت خود بخودی رخ نمی دهند یکی از مسائل مهمی که در واکنش شیمیایی باید در نظر داشت اختلاط مناسب واکنش گر هاست به این معنی که اگر تمام شرایط برای واکنش فراهم باشد ولی مولکول هایی که باید باهم واکنش دهند در کنار یکدیگر قرار نگیرند واکنش رخ
نمی دهد.
اسلاید 8 :
به همین منظور در بعضی از موارد برای اینکه توزیع یکنواختی از واکنشگرها در کنار
هم بوجود آورند بطریقی مخلوط واکنش را هم می زنند. به این ترتیب علاوه بر اینکه مولکولهای
واکنشگرها بدلیل توزیع یکنواخت غلظت در کنار هم قرار گیرند با توزیع یکنواخت دما امکان برخوردهای مٶثرو درنتیجه وقوع واکنش افزایش می یابد تا اینجادیدیم که در انجام واکنش شیمیایی, عوامل متعددی مثل برخورد اتمها ,دما,فشار,اختلاط , کاتالیست و...... تٲثیردارند. برای فراهم شدن شرایط مطلوب جهت انجام واکنش احتیاج به ظرفی داریم تا واکنش در آن انجام شود که در صنعت به این ظرف راکتور گویند. برای ورود مواد اولیه به راکتور در یک کارخانه شیمیایی دستگاه های زیادی وجود دارند تا شرایط مواد اولیه را برای تولید محصول آماده کندو نیز دستگاه های متعدد دیگری وجود دارند تا محصولات خروجی از راکتورها طی یک مجموعه فرآیند به خلوص مطلوب رسانده وآنرا آماده برای مصرف کنند. در نتیجه تمام دستگاه ها به نوعی با عملکرد راکتور ارتباط مستقیم دارند و می توان بیان کرد که راکتور قلب این مجموعه فرآیندی است و عملکرد درست آن اهمیت زیادی در بازدهی کارخانه دارد و مهمترین دستگاه فرآیند محسوب می شود.
اسلاید 9 :
کاربرد آب در صنعت:
یکی از مهمترین کاربردهای آب در صنعت خنک سازی است به عنوان مثال وقتی دستگاهی شبیه موتور و کمپرسور کار می کند بر اثر اصطحکاک حرارت زیادی تولید می شود وقسمتی از حرارت ,به داخل جداره سیلندر ,پیستون وسوپاپ ها منتقل می شود که باید این حرارت تولید شده به وسیله مادهای از آن گرفته شود در موتور های دیزلی این خنک سازی با آب انجام می شود زیرا اگر این حرارت خارج نشود قطعات دچار خستگی و ترک خوردگی زودرس
می شوند . در صنایع و واحدهای پتروشیمی نیز بعضی از واکنش ها در داخل راکتور صورت می گیرد. و تولید حرارت می کند. به منظور کنترل و تثبیت دمای واکنش ,این حرارت تولید شده را بایستی توسط آب از سیستم خارج نمود علاوه بر این ,در بسیاری از تجهیزات فرآیندی مانند مبدل حرارتی برای سرد سازی محصولات , از آب به عنوان میان خنک کننده استفاده می شود.
اسلاید 10 :
در تجهیزاتی که از روغن برای سرد کردن ,یا تا قانهای موتور یا توربین و سایر قطعات استفاده می شود ,در انتها خنک سازی روغن, توسط آب انجام می شود و روغن پس از خنک شدن مجدد در مسیر گردش قرار می گیرد.
آب درصنعت بصورت وسیعی جهت خنک سازی استفاده می شود . در فرآیند سرد سازی ,به اصطلاح به ماده ای که حرارت از دست می دهد ماده سرد شده یاCooled وبه آب که حرارت را جذب می کند , سرد کننده یا Coolent می گویند. آب یک مایع بی بو و بی رنگ در دمای معمولی محیط است , که در مقایسه با سایر مواد برای جوش آمدن و تبخیرشدن احتیاج به میزان حرارت زیادی دارد. به عبارت دیگر می توان گفت که آب قابلیت جذب گرمای بیشتری را دارد وبه همین علت , از آن به عنوان یک سیال مناسب جهت انتقال حرارت می توان استفاده کرد .