بخشی از پاورپوینت
اسلاید 1 :
نقطه ذوب
- پیش زمینه و تئوری
- استفاده ها
- تکنیک های اندازه گیری و ابزار
- محدوده نقطه ذوب
- محدوده نقطه ذوب مواد شناخته شده مخلوط و مجهول
اسلاید 2 :
تئوری و زمینه
نقطه ذوب
- دمایی است که در آن تبدیل فاز بین جامد و مایع اطفاق می افتد.
- دمایی است که در آن بین کریستالهای منظم و جامد و حالت قرار گرفتن شانسی در مایع تعادل وجود دارد.
محدوده نقطه ذوب
- اولین نقطه (دمای پایین ) دمایی است که اولین قطره مایع در بین کریستالها تشکیل میشود.
- نقطه دوم ( دمای بالا) دمایی است که کل توده جامد به مایه شفاف تبدیل میشود.
استفاده
- شناسایی مواد
- اثبات خلوص ماده
اسلاید 3 :
بخش تجربی
تعیین نقطه ذوب برای
دو ترکیب شناخته شده
مخلوطی از دو ترکیب شناخته شده
یک ترکیب ناشناخته
مخلوطی از یک ترکیب ناشناخته و شناخته شده
2تشخیص ترکیب ناشناخته.
وسایل و ابزار
1لوله مویین
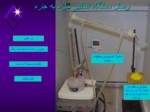
2دستگاه نقطه ذوب
اسلاید 4 :
روش کار
آوردن:
- تهیه دستگاه تعیین نقطه ذوب از اتاق تجهیزات
- انتخاب دو ترکیب با نقطه ذوب شناخته شده
- آوردن ماده ناشناخته از اتاق تهیه
(توجه :شماره ترکیب ناشناخته رادر دفتر یادداشت بنویسید)
پرکردن لوله مویین
- با سر پهن اسپاتول نمونه را بصورت پودر در آورید
- قسمت باز لوله مویین را وارد نمونه کنید(1-2 میلی متر از نمونه)
- از طرف بسته لوله مویین آنرا داخل یک لوله شیشه ای بیاندازید تا نمونه در طرف بسته لوله مویین جمع شود. اگر لازم باشد این عمل را تکرار کنید.
اسلاید 5 :
.3بدست آوردن محدوده نقطه ذوب
لوله مویین را در دستگاه نقطه ذوب قرار دهید.
افزایش دمای دستگاه را به گونه ای تنظیم کنید که 2-3 درجه در دقیقه بالا برود.
تعیین نقطه ذوب تقریبی
اجازه دهید سرد شده و محتویات آن نیمه جامد شود.
دستگاه نقطه ذوب را
اجازه دهید دمای دستگاه 10 درجه پایین بیاید.
دستگاه را دوباره تنظیم کنید که دمای آن 5/0 درجه در دقیقه بالا رود.
محدوده نقطه ذوب را بدست آورید .
اسلاید 6 :
.4لوله مویین را بصورت زیر تهیه کنید:
دو ماده معلوم
نمونه ای مخلوط 1:1 از دو ماده معلوم.
نمونه ترکیب مجهولو
.5محدوده نقطه ذوب هر نمونه را تهیه کنید.
از روی جدول نزدیک ترین نقطه ذوب به نقطه ذوب نمونه را بدست میآوریم.
مخلوط 1:1 نمونه را درست میکنیم
.7رنج نقطه ذوب مخلوط شناخته شده / ناشناخته را تعیین میکنیم.
.8اگر اختلاف نقطه ذوب مخلوط و ترکیب ناشناخته بیش از چند درجه باشد مخلوط دیگری تهیه و نقطه ذوب آنرا تعیین میکنیم.
.9این فرآیند را با مواد شناخته شده دیگر ادامه میدهیم تا اختلاف به حداقل برسد.
اسلاید 7 :
آزمایشگاه مبانی شیمی آلی
تقطیر ساده و جزء به جزء
تقطیر یک تکنیک خالص سازی است که در آن ترکیباتی با نقطه جوش متفاوت با استفاده از کنترول حرارتی از هم جدا میشوند.بخاراتی که در اثر حرارت مناسب ایجاد میشوند توسط یک مبرد جمع آوری شده و نسبت به مخلوط اولیه خالص تر هستند.
مخلوط متانول/آب برای مقایسه کارایی از طریق هر دو روش تقطیر میشود و در بار دوم با قرار دادن ستون تقطیر جزء به جزء با روش اول مقایسه میشود.
اسلاید 8 :
تقطیر ساده در مقابل تقطیر جزء به جزء
- در حالت ایده ال بطور موثری مایعات را بر اساس افزایش نقطه جوش از هم جدا میکند.
- در حقیقت در اغلب موارد جدا سازی ناقص است( هم پوشانی دارد) مخصوصا در مواردی که نقطه جوش
مواد به هم نزدیک باشد یا ابزار های مورد استفاده قدرت جدا سازی کافی نداشته باشد.
- نوعا انتظار داریم که برای اجرای یک تقطیر خوب تغییرات رنج نقطه جوش بین 2-5 درجه باشد
(پهن شدن بیشتر این رنج نشان دهنده مواد با خلوص کمتر میباشد).
اسلاید 9 :
تقطیر جزء به جزء
فاکتور های تاثیر گذار روی کارایی تقطیر:
(چگونه تقطیر در خالص سازی نمونه کمک میکند)
اسلاید 10 :
آزمایشگاه مبانی شیمی آلی
استخراج داروهای ضد درد
استخراج یکی از تکنیک های جدا سازی میباشد که در آن ترکیباتی با حلالیت های متفاوت با استفاده از حلالهایی با قطبیت مختلف جدا سازی میشود.این فرایند شیمیایی اساسی اغلب در واکنشهای اسید باز قابل برگشت
انجام میگیرد.