بخشی از مقاله
دراين تحقيق ،رنگدانه قرمز باپايداري دمايي وشيميايي مناسب براي صنايع پرسلان وتک پخت به روش خوداحتراقي محلول سنتز شد. باجانشيني يون هايکروم که به عنوان عامل رنگ کننده افزوده ميشود،درساختارپروسکايت وتشکيل محلول جامد رنگدانه قرمزي باپايداري دمايي بالا ساخته شد. ابتدا،تأثيرکانيسازهاي مختلف برتشکيل فاز موردبررسي قرارگرفت و باانتخاب سيستم مناسب کانيسازدماي سنتزتا C ١٤٠٠کاهش يافت . سپس اثرميزان کروم نفوذکرده (y)درساختارپروسکايت تعيين شد. بيشترين قرمزي (*a)در٠٠٣=y ديده شد. درنهايت به منظوربررسي پايداري رنگدانه درلعاب هاي دمابالا ودماپايين ،لعاب هاي رنگي حاوي ٥درصد وزني رنگدانه ،تهيه وبرروي بدنه هاي مناسب اعمال گرديد. نتايج رنگ سنجي برروي لعاب هاي پخته شده ،حاکي ازتشکيل رنگ مناسب ،حتي دردماهاي بالاميباشد. درلعاب کاشي ديوار بادماي پخت C ١٠٥٠،مقدار *a دربدنه تهيه شده ، ٣٤,٥٤٩ ودرلعاب دمابالا، ٢٣,٠٢٧به دست آمد.
واژه هاي کليدي :رنگدانه قرمز،پروسکايت ،آلومينات ايتريم ،خوداحتراقي محلول .
١مقدمه
امروزه استفاده ازموادسراميکي جديد درساخت رنگدانه هايي بادماي کاربردبالاتراز 1200C ومقاومت شيميايي مناسب گسترش زيادي يافته است . رنگدانه قرمزباساختارپروسکايت که به وسيله مقدارکمي 3+Cr به عنوان عامل رنگ کننده دوپ شده است علاوه بر داشتن پايداري دمايي وشيميايي مناسب ،برخلاف رنگدانه هاي قرمزي که مصرف مي شود (سولفوسلنيد کادميم حفاظت شده توسط زيرکون ) مسأله آلودگي محيط زيست رانيزندارد. باتوجه به وجود کوئورديناسيون هشت وجهي درساختارپروسکايت آلومينات ايتريم در اثرحضوريون هاي 3+Cr درفضاهاي هشت وجهي اکسيژن وانتقالات الکتروني بين الکترون هاي اوربيتال d درکروم که انرژي نسبتاًبالايي دارند،فام قرمزايجادمي شود. درضمن دماي بالاي سنتز (1400C) ازحضور 5+Cr سمي جلوگيري مي کند [٤-١].
ساختارپروسکايت بدون حضورکاني سازدردماهاي بالاتراز 1600Cبازمان هاي گرمايش طولاني تشکيل مي شود. ولي با استفاده ازيک کاني سازکه درتسريع سنتزبسيارمؤثراست ،مي توان دماي واکنش رابه مقدارقابل توجهي کاهش داد. بنابراين ،انتخاب کاني سازمناسب درسنتزرنگدانه قرمزباساختارپروسکايت بسيارمهم وحياتي مي باشد [٥،٦].
براي سنتزرنگدانه هاي سراميکي ،ازروش هاي مختلفي مانند واکنش حالت جامد،هم رسوبي ،سل ژل وخوداحتراقي استفاده مي شود. استفاده ازروش هاي شيميايي درسنتزپودرهاي سراميکي مزايايي ماننديکنواختي بالاترمحصول ،کاهش دماي سنتز وعدم حضورناخالصي هارادرپي دارد [٧].
درفرآيند خوداحتراقي محلول که اخيرًاگسترش يافته است ، محلول هاي آبي ازنيترات هاي فلزات وسوخت هاي مناسب گرم مي شودتابه ژل غليظي تبديل گردد.دراين حالت احتراق انجام مي شود وخاکستربه جاي مانده ترکيب موردنظرمي باشد. بااين روش تهيه مواداکسيدي باترکيب موردنظر وساختاردلخواه (اسپينل ،پروسکايت ،گارنت و....) امکان پذيراست .
به طورخلاصه مزاياي روش سنتزاحتراقي محلول شامل مواردزير است [٧]:
١به علت حل شدن مواداوليه درآب ،اختلاط مواداوليه درمقياس مولکولي امکان پذيراست . بنابراين ،تشکيل ترکيب موردنظردر مقياس نانومتري امکان پذيرمي باشد.
٢دماي بالاي واکنش باعث توليد ماده اي خالص وبلوري مي شود.
ضمن اينکه دماي بالا به همراه سرعت سرمايش سريع ،باعث مي شودتابتوان به فازهاي دمابالادست پيداکرد.
٣زمان کوتاه فرآيند وتشکيل محصولات گازي درحين واکنش احتراق ،مانع ازرشد ذرات شده وباعث تشکيل پودربااندازه نانومتري وسطح ويژه بالامي شود.
٤ساده بودن تجهيزات مورداستفاده دراين روش ،هزينه نسبتاًکم مواداوليه ،تک مرحله اي بودن فرآيند سنتز وصرفه جويي درانرژي ازمزيت مهم ديگرمي باشد.
نوع سوخت ،نسبت سوخت به اکساينده ،مقدارآب موجوددرآب محلول پيش ازاحتراق ،استفاده ازاکسيدکننده اضافي ، pH محلول و دماي احتراق ازعوامل مؤثردراين روش مي باشند [٩، ٨].
ماده اکسيدکننده (معمولاًنيترات فلزي درسوختن با آزادکردن اکسيژن (ازدست دادن الکترون ) احيامي گردد وسوخت با شکستن پيوندهاي C-H يابه دست آوردن الکترون اکسيد مي شود. در ميان سوخت هاي معمول درروش خوداحتراقي اوره ،اسيد سيتريک ، گلايسين ،کربوهيدرازيد به دليل فراواني وقيمت کمترکاربردبيشتري پيداکرده اند.
تمام سوخت هاي آلي دوويژگي مشخص دارند: همگي منبع کربن وهيدروژن مي باشند ودرهنگام احتراق به H2O و C2O تبديل مي شوند وگرماآزادمي کنند. همچنين اين سوخت هابايون هاي فلزي کمپلکس تشکيل مي دهند وموجب يکنواختي بهترکاتيون هادر محلول مي شوند [٩،١٠].
دراين تحقيق ،رنگدانه قرمزباپايداري دمايي وشيميايي مناسب براي صنايع پرسلان وتک پخت به روش خوداحتراقي محلول سنتز شد. تأثيريون هاي کروم به عنوان عامل رنگ کننده درساختار پروسکايت YAlO3 وتشکيل محلول جامد
(٠١-٠٠١=y)رنگدانه قرمزي باپايداري دمايي بالابررسي شد.
همچنين آزمايشات رنگ سنجي برروي لعاب هاي پخته شده انجام گرديد.
٢بخش تجربي
٢١موادشيميايي ووسايل
دراين تحقيق ازموادشيميايي نيترات ايتريم ،اکسيد ايتريم (Y2O3؛Merck،خلوص :٩٩,٩٩%)،اسيد نيتريک ،نيترات آلومينيوم ،خلوص :٩٩,٩%)،نيترات کروم خلوص :٩٩,٩%)،اسيد سيتريک ( Merck،خلوص ٩٩,٩%)وآمونياک وازدستگاه هاي پراش اشعه X مدل D٥٠٠ زيمنس ،ميکروسکوپ الکتروني پويشي ساخت کمبريج مدل S٣٦٠ واسپکتروفتومتري Color-Eye مدل A٧٠٠٠ساخت شرکت گرتگ مکبس ١استفاده شد.
٢٢روش کار
درابتدا،براي توليد نيترات ايتريم ،اکسيد ايتريم به کمک همزن مغناطيسي ودماي 50Cدر 2mLاسيد نيتريک %٦٥حل شد.
سپس مقاديرنيترات آلومينيوم ونيترات کروم طبق استوکيومتري توزين شد وبه طورجداگانه در 50mL آب مقطرحل شدند. محلول هاي شفاف به دست آمده پس ازمخلوط شدن به مدت ٣٠دقيقه برروي همزن مغناطيسي قرارگرفتند تا کاملاًيکنواخت شود. ازاسيد سيتريک به عنوان سوخت استفاده شد.
نسبت مولي اسيد سيتريک به يون هاي فلزي درمحلول ١:١انتخاب گرديد. اسيد سيتريک پس ازحل شدن درآب مقطربه صورت قطره قطره باکمک بورت به محلول اضافه شد. اسيد سيتريک در pH خنثي مي تواند تقريباًبه طورکامل پروتون هاي خودراآزادکند وبا کاتيون هاي فلزي کمپلکس تشکيل دهد. اين امرمانع ازهيدراته شدن ورسوب دادن ترکيبات موجوددرمحلول مي شود. باافزودن آمونياک به صورت قطره قطره وآهسته pH محلول به حدود ٧رسيد. باتنظيم دماي هيتردر 100C،آب محلول تبخيرشد ومحلول غليظ گرديد.
باافزايش دماي هيتربه 450Cژل شروع به جوشيدن وبالاآمدن کرد.سپس واکنش احتراق اتفاق افتاد.پس ازچند ثانيه پودري نرم و متخلخل به دست آمد. پودرحاصل ازاحتراق به همراه کاني سازدر هاون عقيق مخلوط وسپس دربوته هاي آلومينايي دربسته ريخته شد وپس ازکلسينه کردن در 1400Cبه مدت ٤ساعت وباسرعت گرمايش 10C/minدراتمسفرهوا،رنگدانه قرمزحاصل شد.
سيستم هاي کاني سازبه کاررفته دراين مطالعه ودماي ذوب آنها درجدول ١آمده است . اين کاني سازهابه ميزان ثابت ٦% وزني به پودر حاصل ازاحتراق بامقاديرمختلف کروم (٠,٠١تا ٠,١مول ) افزوده شدند. درنهايت براي ارزيابي پايداري رنگدانه هاي سنتزشده ، ٥% وزني ازآنهابه دولعاب شفاف صنعتي يکي لعاب کاشي ديواربادماي پخت
1050C وديگري لعاب بدنه چيني بهداشتي بادماي پخت 1200C ، افزوده شد. ترکيب حاصل همراه آب به مدت ٣٠دقيقه يکنواخت و دوغاب حاصل برسطح بدنه هااعمال شد.
فازهاي تشکيل شده دررنگدانه هاي کلسينه شده توسط دستگاه پراش اشعه X باپرتو به طول موج ٠,١٥٤٢نانومتردرمحدوده بررسي شدند.
براي بررسي مورفولوژي ،توزيع وشکل فازهاازدستگاه ميکروسکوپ الکتروني پويشي استفاده شد.
بااستفاده ازدستگاه اسپکتروفتومتري Color-Eye پارامترهاي رنگ سنجي درسيستم CIE-Lab درمحدوده طول موج nm٧٥٠-٣٦٠ بربدنه هاي لعاب خورده اندازه گيري شد.
٣نتايج وبحث
٣١اثرکاني سازبرتشکيل ساختارپروسکايت YAlO3
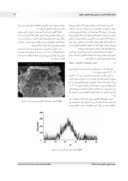
باتوجه به نمودارفازسيستم تشکيل ساختارپروسکايت بدون حضورکاني سازدر C ١٤٠٠امکان ندارد. بنابراين ،انتخاب کاني سازمناسب درسنتزرنگدانه قرمزباساختارپروسکايت بسيارمهم وحياتي مي باشد. الگوي پراش اشعه ايکس نمونه هاي سنتزشده با استوکيومتري باکاني سازهاي مختلف درشکل ١ نشان داده شده است . اين نمونه هادر C ١٤٠٠وبه مدت ٢ساعت کلسينه شده اند.
بابررسي الگوهاي به دست آمده ،مشخص شدکه درنمونه هاي
M1 تا M6فازهاي نامطلوب (مکعبي ) و (تتراگونال ) فازهاي اصلي سيستم هستند. درنمونه M٧ که درآن از کاني ساز ٢ استفاده شده است ،حضورفاز پروسکايت مشاهده مي شود.
همان طورکه ذکرشد،فازپروسکايت نمي تواند به صورت تعادلي دردماي C ١٤٠٠وجودداشته باشد. ازطرفي ،تبلورازفازمايع مي تواند غيرتعادلي باشد. بنابراين به نظرمي رسدکه کاني سازهابا تشکيل فازشيشه مي توانند اجزاء Al و Y رادرخودحل کرده وپس ازبه اشباع رسيدن فازمايع ،به صورت YAlO3 رسوب کند. به عبارت ديگر YAlO3 به صورت غيرتعادلي رسوب مي نمايد. مقدار وزمان تشکيل فازشيشه وگرانروي آن مي تواند دراين فرآيند مؤثرباشد.
افزودني NaF به سرعت تبخيرمي شود وسيستم راترک مي کند.
بالعکس MgF2 به آهستگي تبخيرمي شودولي دماي ذوب بالاتري دارد (C ١٢٧٠). فلزات قليايي گرانروي مذاب راکاهش مي دهند. در اين ميان ليتيم به علت کوچک بودن وشدت ميدان بالاتر،تأثير بيشتري درکاهش گرانروي مذاب خواهد داشت [٦].