بخشی از پاورپوینت
--- پاورپوینت شامل تصاویر میباشد ----
اسلاید 1 :
جلسه اول:
فهرست مطالب
مقدمه
جايگاه مفهوم و قواعد رزونانس در شيمي آلي
اصول و قواعد رسم فرم هاي رزونانسي
چگونه مي توان فرم هاي رزونانسي ارجح را تشخيص داد؟
خصلت اسيديته و مفهوم رزونانس
خصلت بازيسيته و مفهوم رزونانس
اسلاید 2 :
رزونانس، جابجائي الکترون هاي غير مستقر مي باشد و هنگامي پر رنگ تر جلوه مي نمايد که اربيتالهاي غير پيوندي پي مربوط به کربانيونها يا کربوکاتيونها در مجاورت پيوندهاي چندگانه يا هترو اتم هاي داراي زوج الکترنهاي غير پيوندي موجود باشد.
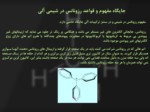
اتم هائي که در رزونانس شرکت مي کنند بايد در يک صفحه قرار گرفته و اربيتال هاي رزونانس دهنده آنها موازي همديگر قرار گيرند. به عنوان مثال در كاتيون تري متيل فنيل زير كربن مركزي و هر كدام از حلقه ها در يك صفحه اند ولي سه حلقه بنزن به دليل ممانعت فضايي نمي توانند هر سه در يك صفحه باشند بنابر اين، كاتيون كربن مركزي نمي تواند همزمان با هر سه حلقه رزونانس داشته باشد.
اسلاید 3 :
انرژي رزونانسي:
اختلاف بين انرژي محاسبه شده حالت مستقر (هر يک از فرم هاي رزونانسي) ، Ec و انرژي حالت واقعي مولکول (انرژي هيبريد رزونانس) ،Eh مي باشد، كه انرژي هيبريد رزونانس Eh هميشه کمتر از انرژي محاسبه شده براي هر يک از فرم هاي رزونانسي، Ec مي باشد
رزونانسي در بعضي از ترکيبات موجب افزايش پايداري و به دنبال آن کاهش واکنش پذيري مي گردد. مثلا در ترکيبي مثل بنزن، رزونانس موجب کاهش انرژي آن نسبت به هگزاتري ان شده است، در برخي موارد نيز (مثل ترکيبات آنتي آروماتيک) رزونانس موجب ناپايداري ترکيب مي گردد. در موارد زير رزونانس موجب ناپايداري مي گردد:
حلقه شش تائي وسط در ترکيب شماره (3) بدليل عدم امکان رزونانس، داراي پيوندهاي مستقر بوده و سيکلوهگزاتري ان است و بنزن نمي باشد (زيرا با رزونانس اين حلقه، حلقه هاي چهارتائي آنتي آروماتيک مي شوند).
اسلاید 4 :
جابجا کردن يک جفت الکترون از يک اتم و دور کردن آن از ديگري منجر به جابجا شدن بار مي شود:
2. هنگام نوشتن فرم هاي رزونانسي مکانهاي نسبي همهء اتم ها بدون تغيير مي ماند.
به عنوان مثال، فرم (C) در شكل زير غلط است زيرا در آن اتم ها جابجا شده اند.
3. ساختمانهاي رزونانسي معادل (هم ارز) سهم يکساني در هيبريد رزونانسي دارند .
اسلاید 5 :
4. فلش هائي که فرم هاي رزونانسي را به هم مربوط مي سازند، يك فلش دوطرفه مي باشد. يعني فلش هائي نيستند كه بيانگر تعادل () باشند. زيرا در تعادل گونه هاي سمت راست و سمت چپ فلش ها همه وجود دارند، اما در اينجا هيچکدام از اين فرم هاي رزونانسي وجود ندارند و فرم هيبريدي در واقع در بردارنده همه فرم هاي رزونانسي مي باشد و هيبريد رزونانس است که وجود دارد.
نكته : هرچه تعداد فرم هاي رزونانسي بيشتر باشد، پايداري گونه و يا حدواسط بيشتر است. زيرا آنتروپي افزايش يافته و انرژي آزاد گيبس کاهش مي يابد.
ΔG = ΔH – TΔS
5. امکان دارد براي يک گونه (يون يا مولکول)، تمامي فرم هاي رزونانسي که مي توان نوشت هم ارز نباشند، در اينصورت اگرچه همه فرم ها در ساختمان هيبريدي سهيم هستند ولي سهم فرم ارجح بيشتر است، و همهء فرم هاي رزونانسي سهم يکسان در ساختمان هيبريدي ندارند .
اسلاید 6 :
1. فرم هاي رزونانسي که در آنها همه اتم ها اکتت هستند و ماکسيمم پيوند کوالانسي وجود داشته باشد، فرم ارجح است.
به عنوان مثال فرم هاي شماره (1) در مثال هاي زير بدليل اکتت بودن همه اتم ها و دارا بودن ماکسيمم تعداد پيوند در ساختار خود ارجح بوده و سهم بيشتري در فرم هيبريد رزونانسي دارند.
2. ساختارهائي که داراي بار قرادادي کمتري باشند، پايدارترند. يا به عبارت ديگر ساختارهاي رزونانسي كه کمترين جدائي بار را داشته باشند، ارجح مي باشند. به همين دليل ساختمان هاي خنثي بهتر از فرم هاي دو قطبي مي باشند، زيرا در اينگونه ساختارها جدائي بار وجود ندارد.
اسلاید 7 :
ساختار(A) پايدارترين فرم رزونانسي است چون فاقد بار قراردادي است، فرم (C) نيز بدليل اينکه اتم کلر داراي اربيتال d است، مشاهده مي گردد. بنابراين اگر در اين ترکيب به جاي کلر، فلوئور داشته باشيم، فرم(C) مشاهده نمي شود.
3. اگر تمام ساختارهاي يك تركيب بار قراردادي داشته باشند، پايدارترين آنها (کم انرژي ترين) ساختاري است که بار منفي روي اتم الکترونگاتيوتر و بار مثبت روي اتم الکتروپوزيتيوتر قرار داشته باشد.
بنابراين در مورد دوم ساختار (1) از همه پايدارتر است زيرا بار قراردادي ندارد و از بين ساختارهاي (2) و (3) نيز ساختار (2) پايدارتر است، زيرا بار منفي روي اتم الکترنگاتيوتر قرار دارد.
اسلاید 8 :
بطور کلي بايد پايداري آنيون حاصل از جدا شدن پروتون (پايداري باز مزدوج) را در نظر گرفت. هر چه اين آنيون به وسيله پخش بار پايدارتر شود، خصلت اسيديته ترکيب بيشتر مي باشد و واکنش براي تفکيک پروتون مساعدتر است.
مثال:
در مثال بالا قدرت اسيدي ترکيب (2) بيشتر از ترکيب (1) است، زيرا بار منفي توليد شده در تركيب (2) توسط رزونانس پخش و پايدار شده است .
اما در مثال بالا در اثر رزونانس بار منفي به اتم الکترونگاتيو (اکسيژن) منتقل مي گردد و علاوه بر رزونانس، اثر القائي اتم الکترونگاتيو موجب افزايش قدرت اسيدي (3) نسبت به ترکيب شماره (2) در مثال فوق مي گردد .
اسلاید 9 :
در اثر جدا شدن پروتون هاي مشخص شده و رزونانس مربوطه بار منفي ايجاد شده با آروماتيک نمودن حلقه پنج عضوي پايدار مي گردد. بنابراين قدرت اسيديته اين پروتون ها از پروتون هاي آليليک معمولي بيشتر است.
اسلاید 10 :
اختلاف اسيدي دو ترکيب به خاطر آروماتيک شدن دي ان حلقوي بر اساس قاعده هوکل (4n+2)πe مي باشد. اگر چه تعداد ساختارهاي رزونانسي براي هر دو يکسان است