بخشی از مقاله
مارکر PS٥٠٤ در تشخيص پروليفراسيون غددي آتيپيک پروستات
چکيده
زمينه و هدف: تاکيد بر کشف زود هنگام سرطان پروستات به کمک اولتراسونوگرافي ترانس رکتال و بيوپسي سوزني ، پاتولوژيست ها را با معضل تشخيص سرطانهاي کوچک مواجه نموده است . اخيرا̋ از مارکر PS٥٠٤ جهت تشخيص قطعي سرطان در بيوپسي هاي کوچک استفاده شده است . روش بررسي : رنگ آميزي مارکر PS٥٠٤ براي ٧٠ نمونه بيوپسي سوزني پروستات و شش نمونه رزکسيون از طريق مجرا که همگي حاوي کانونهاي مشکوک (آتيپيک ) بودند و نيز٤٠ نمونه سرطان قطعي پروستات، شامل هشت نمونه داراي سلولهاي کف آلود (foamy) به عمل آمد. يافته ها: ٣٦ نمونه از بيوپسي سرطان قطعي ، درجاتي از رنگ پذيري براي PS٥٠٤ نشان دادند (حساسيت ٩٠%)؛ دو سرطان کوچک و دو سرطان با سلولهاي کف آلود فاقد رنگ پذيري بودند. از مجموع ٧٦ مورد مشکوک، ١٨ مورد به عنوان نئوپلازي داخل اپي تليالي درجه بالا (HGPIN) شناخته شدند که ١٦ مورد آنها رنگ پذيري متوسط منتشر نشان دادند. از ٥٨ مورد باقيمانده داراي پروليفراسيون غدد کوچک آتيپيک ١٤ مورد قويا به نفع سرطان بود که چهار مورد آنها فاقد رنگ پذيري PS٥٠٤ بودند. در بين ٤٤ مورد آتيپيک به نفع خوشخيمي ، ١٤ مورد هيپرپلازي آدنومي آتيپيک با دو مورد رنگ پذيري ضعيف موضعي و دو مورد آتيپي به دنبال پرتوتابي با يک مورد رنگ پذيري موضعي مشاهده شد و ٢٨ نمونه ديگر PS٥٠٤ منفي بودند. نتيجه گيري: حساسيت PS٥٠٤ براي کشف سرطان پروستات از آنچه قبلا تصور مي شد پايين تر است . منفي تلقي شدن سرطانهاي کوچک ممکن است به دليل ناهمگوني رنگ پذيري باشد. در پروليفراسيون غدد کوچک آتيپيک ، رنگ پذيري مثبت و منتشر PS٥٠٤ قويا گوياي تشخيص سرطان است ولي عدم رنگ پذيري آنرا رد نمي کند. حساسيت PS٥٠٤ براي کشف سلولهاي سرطاني کف آلود و کانونهاي کوچک سرطاني کمتر است . HGPIN غالبا̋ رنگ پذيري متوسط منتشر نشان مي دهد. رنگ پذيري ضعيف کانوني ممکن است در غدد خوشخيم نيز مشاهده شود. ما استفاده از *نويسنده مسئول، تهران، ميدان حسن آباد، بيمارستان سينا، PS٥٠٤ را فقط در همراهي با بررسي مورفولوژيک و مارکرهاي سلولهاي بازال توصيه مي کنيم .
مقدمه
اگر چه معاينه دقيق رکتال (Rectal examination) هنوز يک روش کارا و عملي براي کشف کارسينوم پروستات به شمار ميرود، تائيد پاتولوژيک هميشه ضروري است چرا که در معاينه باليني نمي توان سرطانهاي زودرس را با اطمينان از کانونهاي هيپرپلازي ندولار، پروستاتيت گرانولومي ، سل ، انفارکت يا سنگ پروستات افتراق داد. اولتراسونوگرافي ترانس رکتال (TRUS) مي تواند سرطانهاي به کوچکي پنج ميلي متر را کشف کند ولي از تشخيص حدود ٣٠% تومورهاي پروستات که ايزواکو هستند عاجز است و لذا کارآيي آن به عنوان ابزاري براي غربالگري ثابت نشده است .٦-١ در عصر حاضر که غربالگري با آنتي ژن اختصاصي پروستات Prostatic (PSA)Specific Antigen رايج است پاتولوژيست ها به طور روزافزون با نمونه هاي بيوپسي سوزني پروستات حاوي مناطق بسيار کوچک سرطان پروستات مواجه مي شوند.٢و١ تشخيص قطعي يک سرطان محدود پروستات مي تواند يک چالش عمده تشخيص باشد.
مارکرهاي سلولهاي بازال مانند در شناسايي کانونهاي کوچک داراي غدد آتيپيک مفيد هستند.٦-٣ اگر هر دو مارکر سلولهاي بازال گوياي فقدان لايه سلولهاي بازال در غدد آتيپيک باشند گواه سرطان پروستات است ولي تشخيص سرطان پروستات با استفاده از مارکرهاي سلولهاي بازال ممکن است هميشه قطعي نباشد. برخي ضايعات خوشخيم مانند هيپرپلازي آدنومي آتيپيک AAH-Atypical Adenomatous Hyperplasia ، هيپرپلازي متعاقب آتروفي (PAH)Post-Atrophic Hyperplasia و نيز نئوپلازي داخل اپي تليالي با درجه بالا High-Grade Prostatic Intraepithelial (HGPIN)Neoplasia ممکن است رنگ پذيري موضعي يا غير يکنواخت نشان داده و موجب گمراهي در تشخيص شوند.٩-٧ لذا فقدان يک مارکر اختصاصي سرطان پروستات همواره يک محدوديت تشخيصي در آزمايش بافت شناسي معمول به شمار ميرفته است . اخيرا در تجربيات مختلف و به کمک تجزيه و تحليل ميکروآرايه DNA مکمل ، آلفا- متيل استيل – کوانزيم A راسماز (AMACR) به عنوان يک ژن که به طور ثابت در سرطان پروستات فعال شده ولي در بافت خوشخيم پروستات بيان نمي شود در کانون توجهات قرار گرفته است .١٢-١٠ اين ژن يک پروتئين سيتوپلاسمي را که در بتا اکسيداسيون اسيدهاي چرب شاخه دار نقش دارد کد مي کند. يک آنتي بادي تک دودماني براي AMACR تهيه شده است که به نام P504S شناخته مي شود (Zeta, Sierra Madre, CA) و به صورت تجاري در دسترس است و آنرا مي توان روي نمونه هاي بافتي که به طور معمول توسط فرمالين فيکس شده و پارافين اندود شدهاند به کار برد. بررسي هاي اوليه نشاندهنده مفيد بودن AMACR در کشف سرطان پروستات بوده و الگوهاي نحوه بيان آن نيز در تشخيص ضايعات احتمالي زمينه ساز سرطان مانند HGPIN کمککننده بودهاند.١٦-١١ با اين حال هنوز ارزيابي هاي بيشتري از کارايي باليني AMACR در موارد آتيپيکال که از عمدهترين مشکلات تشخيصي پاتولوژيک سرطان پروستات مي باشند مورد نياز است . هدف از اين مطالعه ارزيابي کاربرد تشخيصي P504S در کشف سرطان پروستات در موارد آتيپيک و مشکل در نمونه هاي بيوپسي سوزني و (TURP)Transurethral resection of prostate از جمله در زير گروه نادر غدد کف آلود و يا در مواردي مي باشد که با کانونهاي کوچک مشکوک در بيوپسي سوزني مواجه مي شويم .
روش بررسي
از بين نمونه هايي که ظرف مدت دو سال در بخش پاتولوژي بيمارستان سازمان پزشکي ملي دمنهور مصر آزمايش شده بودند ٧٤ نمونه بيوپسي سوزني و شش نمونه TURP که همگي داراي کانونهاي آتيپيک مشکوک به سرطان بودند انتخاب شدند. چهار نمونه بيوپسي سوزني به علت از دست رفتن کانونهاي آتيپيک در برشهاي عمقي حذف شدند. در ٧٦ مورد باقيمانده، در بررسي معمولي ميکروسکوپي ١٤ نمونه بسيار مشکوک به سرطان پروستات و ٦٢ نمونه تا حدي مشکوک با تشخيص هاي افتراقي AAH،PAH ، HGPIN و آتيپي ناشي از پرتوتابي قرار داشتند. علاوه بر موارد فوق ٤٠ نمونه بيوپسي سوزني سرطان قطعي پروستات نيز به عنوان کنترل انتخاب شدند. اين موارد شامل هشت تومور با ويژگي غالب غدد کف آلود و ١٢ مورد داراي يک کانون کوچک تومورال (کمتر از پنج 17 درصد سطح نمونه بيوپسي ) بودند.
ارزيابي و تجزيه و تحليل ايمونوهيستوشيميايي : از هر نمونه بيوپسي سوزني چهار برش پنج ميکرومتري در دو سطح جهت اسلايد ميکروسکوپي تهيه شد. اسلايدهاي اول و چهارم براي رنگ آميزي H&E و اسلايدهاي دوم و سوم جهت ايمونوهيستوشيمي استفاده شدند. رنگ آميزي استاندارد ايمونوهيستوشيميايي به کمک -ABC-Avidin-Biotin Complex به کار رفت . غلظت آنتي بادي در بهترين حدي تنظيم شد که بتواند قويترين رنگ آميزي سلولهاي هدف بدون رنگ آميزي زمينه را ايجاد کند. به دنبال پارافين زدايي و آبدهي ، به منظور بهترين بازيابي آنتي ژني قبل از رنگ آميزي ايمونولوژيک لامهاي بافتي در ٦٠=PH و بافرسيترات ٠.١ مولار درون بخار پز قرار داده شده و سپس به مدت ١٥ دقيقه با درجه بالا در معرض ميکروويو قرار گرفتند. رنگ آميزي با دستگاه خودکار -DAKO, Carpinteria, CA-Autoimmuno-stainer انجام گرفت برشهاي بافتي با آنتي بادي مونوکلونال خرگوشي PS٥٠٤ با رقت ١:٢٠ و به مدت دو ساعت در دماي اتاق انکوبه شدند. براي مشخص کردن جايگزيني آنتي بادي از روش شناسايي DAKO Envision plus و طبق دستورالعمل مربوطه استفاده شد. برشها پس از شستشو در معرض ديآمينوبنزيدين و آب اکسيژنه به مدت پنج دقيقه قرار گرفته و سپس زمينه با هماتوکسيلين رنگ آميزي شد. رنگ پذيري سيتوپلاسم يا لبه لومينال سلولهاي اپي تليالي به عنوان مثبت تلقي شد.١٢،١٨،١٩ نحوه بيان PS٥٠٤ در ضايعات خوشخيم ، آتيپيک و کاملا بدخيم بر اساس وسعت و شدت رنگ پذيري ارزيابي شد. وسعت رنگ پذيري به صورت منتشر (٥٠%<)، موضعي (٥٠%-٥%)، بسيار کم (٥%>) منفي و شدت رنگ پذيري نيز به درجات ١ (منفي )، ٢ (ضعيف )، ٣ (متوسط ) و ٤ (قوي) درجه بندي شدند.١٩،١٨،١٢ جهت ارزيابي ايمونوهيستوشيميايي سلول بازال، همه نمونه هاي آتيپيک با مارکر سلول بازال 34ßE12 يا anti-P63 4A4 يا هر دو و به روش ABC رنگ آميزي شدند. به دنبال پارافين زدايي و آبدهي ، برشها به مدت ١٥ دقيقه در محلول بافر ١٠ ميلي مولار سيترات (٦٠=PH) درون ميکروويو قرار گرفته و سپس به ترتيب در معرض آنتي بادي اوليه ، آنتي بادي بيوتينه ثانويه ، ABC و سوبستراي کروموژنيک ديآمينو بنزيدين قرار گرفتند. آنتي باديهاي اوليه و غلظت آنها عبارت بودند از (DAKO) ßE٣٤١٢١١٠٠ و همچنين P٦٣١١٠٠ A٤٤ سپس رنگ آميزي زمينه با هماتوکسيلين انجام شد. مارکر ßE٣٤١٢ سيتوپلاسم سلولهاي بازال و مارکر P٦٣ هسته اين سلولها را رنگ مي کند.
تفسير هر دو رنگ سلولهاي بازال با استفاده از معيارهاي از پيش تعيين شده انجام گرفت .٦و٥ به طور خلاصه رنگ پذيري مثبت در مناطق مشکوک به عنوان خوشخيم تلقي شد به شرط آنکه غدد رنگ پذير بخشي از ناحيه مشکوک بوده و غدد سالم به دام افتاده نباشند عدم رنگ پذيري غدد مشکوک نيز گوياي سرطان تلقي شد به شرطي که شواهد مورفولوژيک آنرا تائيد نمايند.
يافته ها
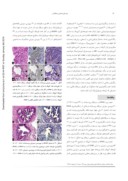
نحوه بروز PS٥٠٤ در سرطان پروستات: در ٣٦ نمونه (٩٠%) از ٤٠ بيوپسي سوزني سرطان پروستات درجاتي از رنگ پذيري P504S ديده شد (جدول ١) ولي چهار نمونه فاقد رنگ پذيري بودند که دو نمونه آن مربوط به سرطان با سلولهاي کف آلود و دو نمونه ديگر مربوط به سرطانهاي کوچکي بود که کمتر از ٥% نمونه را تشکيل مي داد. شدت رنگ پذيري در ٢٤ مورد (٦٧%) متوسط تا قوي و در ١٢ مورد (٣٣%) ضعيف بود. وسعت رنگ پذيري در ١٠ مورد (٢٥%) موضعي يا ناهمگون بود. در نمونه هايي که داراي غدد کف آلود بوده يا داراي کانونهاي کوچک سرطاني بودند، فقدان رنگ پذيري براي مارکرهاي سلول بازال مويد تشخيص سرطان بود (شکل ١، a تا c).
نحوه بروز PS٥٠٤ در ضايعات آتيپيک: از مجموع ٦٢ مورد شامل ٥٦ بيوپسي سوزني و شش TURP که پروليفراسيون آسيني هاي کوچک آتيپيک نشان مي دادند چهار نمونه بيوپسي سوزني به دليل فقدان مناطق مورد نظر در برشهاي عمقي ايمونوهيستوشيمي کنار مجله دانشکده پزشکي ، دانشگاه علوم پزشکي تهران، دوره ٦٦ ،شماره ٢،ارديبهشت ١٣٨٧ گذاشته شدند. از ٥٨ مورد باقيمانده در ١٤ بيوپسي سوزني يافته هاي مورفولوژيک بسيار به نفع سرطان بود (در شش نمونه از اينها يک کانون HGPIN نيز در کنار غدد کوچک آتيپيک ديده شد) و در ٤٤ مورد بقيه شواهد مورفولوژيک به نفع ضايعه خوشخيم بودند .
(جدولهاي ١ و ٢). از بين ١٤ بيوپسي سوزني مشکوک به بدخيمي
شکل - ١: بيوپسي سوزني پروستات. a، يک کانون کوچک سرطان (H&E، ٢٠٠×).
b، منفي شدن غدد آتيپيک با مارکر سلول بازال: سرطان (٢٠٠×). c، رنگ پذيري متوسط منتشر با PS٥٠٤ در اکثر غدد سرطاني (پيکان: رنگ پذيري منفي ، ٢٠٠×). d، غدد کوچک آتيپيک (پيکانها) مشکوک به بدخيمي (H&E، ٢٠٠). e، منفي شدن غدد کوچک (پيکانها) با مارکر سلول بازال: سرطان (٢٠٠×). f، فقدان رنگ پذيري غدد آتيپيک (پيکانها) با PS٥٠٤ (٢٠٠×). عدم تشخيص قطعي با PS٥٠٤.
شکل - ٢: a، نماي HGPIN در بيوپسي سوزني پروستات (H&E، ٤٠٠(. b، رنگ پذيري متوسط ، منتشر و پيراموني لبه غدد (پيکانها) با PS٥٠٤ در HGPIN
(٤٠٠×). c، غدد خوشخيم پروستات در بيوپسي سوزني (H&E، ٤٠٠. d، رنگ پذيري موضعي و غير پيراموني لبه غدد خوشخيم (پيکانها) با PS٥٠٤ (٤٠٠×).
در شش نمونه (٤٢.٨%) رنگ پذيري منتشر P504S و عدم رنگ پذيري مارکر بازال تشخيص بدخيمي را تائيد کردند. در چهار نمونه (٢٨.٦%) غدد آتيپيک براي P504S منفي بودند که منفي بودن توام مارکر سلولهاي بازال مويد تشخيص سرطان بود (شکل ١، d تا f) و در چهار نمونه (٢٨.٦%) که با HGPIN نيز همراهي داشتند رنگ پذيري ضعيف و کانوني P504S در غدد کوچک آتيپيک و همچنين رنگ پذيري غيريکنواخت و ناموزون مارکر بازال هم در غدد کوچک و هم در غدد HGPIN مانع رسيدن به تشخيص قطعي سرطان بود و لذا هيچيک از مارکرها کمکي به تشخيص نکردند (جدول ٢). از ٤٤ مورد که شواهد مورفولوژيک گوياي ضايعه خوشخيم بودند در ٢٢ بيوپسي سوزني (٥٠%) تشخيص PAH داده شده بود در ١٤ مورد (٣١.٨%) که شامل شش TURP بود تشخيص AAH مطرح گرديده بود و چهار نمونه (٩.١%) تحت عنوان پروليفراسيون غدد آتيپيک خوشخيم مشخص شده بودند. دو نمونه (٤.٥%) تحت عنوان هيپرپلازي سلول بازال و دو نمونه ديگر (٤.٥%) به عنوان آتيپي ناشي از پرتوتابي نيز در اين گروه جاي داشتند (جدول ١). در تمامي اين موارد رنگ پذيري سلولهاي بازال ديده شد که گوياي خوشخيمي آنها بود. تمامي موارد PAH و ١٢ مورد AAH از نظر مارکر PS٥٠٤ منفي بودند ولي در دو نمونه از موارد AAH (١٤%) رنگ پذيري ضعيف کانوني ديده شد. در يک بيوپسي سوزني به دست آمده از بيماري که تحت راديوتراپي قرار گرفته بود رنگ پذيري کانوني PS٥٠٤
ديده شد ولي در عين حال رنگ پذيري همين غدد کوچک با مارکر بازال به نفع خوشخيمي و تغييرات ناشي از پرتوتابي بود.
نحوه بروز PS٥٠٤ در HGPIN: از مجموع ٨٠ مورد آتيپيک، ١٨ بيوپسي سوزني HGPIN مشاهده شد که از اين بين ١٦ مورد آنها (٨٩%) درجاتي از رنگ پذيري PS٥٠٤ نشان مي دادند. در ١٢ نمونه (٧٥%) رنگ پذيري به صورت منتشر، متوسط ، پيراموني و يا قطعه اي در لبه درون مجرايي سلولها مشاهده شد و در چهار نمونه (٢٥%) رنگ آميزي PS٥٠٤ به صورت کانوني و ضعيف بود (شکل ٢، a و b).
نحوه بروز PS٥٠٤ در غدد خوشخيم پروستات: در مجموع ٧٦ نمونه مجله دانشکده پزشکي ، دانشگاه علوم پزشکي تهران، دوره ٦٦
مشکوک به بدخيمي که براي مارکر P504S رنگ آميزي شده بودند نحوه رنگ پذيري غدد خوشخيم نيز بررسي شد که در ٢٠ مورد (٢٦%) رنگ پذيري ضعيف و به ندرت متوسط و غير پيراموني در لبه غدد مشاهده شد. اين الگوي رنگ آميزي به عنوان غير اختصاصي در نظر گرفته شد و مشکل تشخيص ايجاد نکرد (شکل ٢، c و d).
بحث
تشخيص سرطان پروستات در نمونه هاي بيوپسي سوزني بر پايه مجموعه اي از ويژگي هاي مورفولوژيک داده مي شود و اگر فقط يک کانون کوچک مشکوک به سرطان در نمونه وجود داشته باشد تشخيص با مشکل مواجه مي گردد.٢٠ در اين گونه موارد به طور گستردهاي از مارکرهاي سلول بازال مانند 34ßE12 و اخيرا پروتئين هسته اي P63 به عنوان ابزار کمک تشخيصي مورفولوژيک استفاده شده است .٦-٣ اين ابزارهاي مفيد محدوديت هايي نيز دارند. بسياري از ضايعات آتيپيک خوشخيم مانند AAH،PAH و HGPIN رنگ پذيري پراکنده يا منقطع نشان مي دهند که تفسير آنها را مشکل مي سازد.٩-٧ به علاوه کاملا ثابت شده است که رنگ پذيري 34ßE12 به نحوه فيکساسيون با فرمالين و روشهاي ايمونوهيستوشيميايي مانند نحوه بازيابي آنتي ژن بسيار حساس بوده و تغييرات حاصله مانند از دست رفتن رنگ پذيري غدد خوشخيم يا رنگ پذيري قطعه اي آنها گاهي منجر به تشخيص اشتباهي سرطان پروستات در ضايعات خوشخيم مي گردد.٢١ لذا بسياري از پاتولوژيست ها اکراه دارند که يک تشخيص مثبت سرطان را بر پايه يک واکنش منفي ايمونوهيستوشيمي مطرح سازند. در جستجو براي يافتن يک بيومارکر قابل اعتماد و اختصاصي براي سرطان پروستات، AMACR توجه فراواني را برانگيخته و دورنماي يک بيومارکر بافتي عالي را به نمايش مي گذارد. تجزيه و تحليل آماري ديفرانسيل به دست آمده از نحوه بروز چهار ژن در سرطان پروستات نشاندهنده اين است که ژن AMACR که در بافت خوشخيم پروستات بيان نمي شود در سرطان به طور ثابت بروز مي يابد.١٢-١٠ Jiang و همکاران١٣ نشان دادند P504S که يک آنتي بادي مونوکلونال براي AMACR است يک مارکر حساس و اختصاصي براي سرطان پروستات بوده و مي توان آنرا به روشهاي معمول ايمونوهيستوشيمي بر روي برشهاي بافتي فيکس شده با فرمالين و پارافين اندود به کار برد. اين گروه در تمامي موارد قطعي سرطان پروستات رنگ پذيري قوي گرانولارسيتوپلاسمي PS٥٠٤ ديدند که در ٧٥% آنها صرفنظر از درجه بندي گليسون وسعت رنگ پذيري به صورت منتشر بود.١٣ اين گروه همچنين بروز PS٥٠٤ را در HGPIN و در ١٢% غدد خوشخيم که فقط به صورت موضعي يا ضعيف بود گزارش کردند. Jiang بعدها پي برد که حساسيت PS٥٠٤ براي کشف کانونهاي کوچک سرطان در بيوپسي هاي سوزني کمتر (٩٤.٥%) بوده و در هيچ يک از ٦٩ غده خوشخيم پروستات ديده نشد.١٦ همچنين روبين ١٢ با آزمايش روي تعداد زيادي نمونه نشان دادند که در سرطان پروستات کپي برداري و پروتئين سازي از روي ژن AMACR افزايش مي يابد. آنها با استفاده از يک آنتي بادي پلي کلونال در ٦٨ مورد از ٧٠ نمونه بيوپسي سوزني پروستات فعاليت شديد AMACR را مشاهده کرده و حساسيت ٩٧% و ويژگي ١٠٠% را براي اين روش بيان کردند.١٢ بعدها Zhou و همکاران ١٩ گزارش دادند که بيان AMACR براي پروستات اختصاصي نبوده و در تعدادي از سرطانها شامل کولورکتال، پستان، تخمدان و ملانوما نيز افزايش مي يابد.١٩ LUO و همکاران ١١ نيز با استفاده از يک کوکتل آنتي بادي شامل AMACR و P٦٣ مفيد بودن AMACR را خاطر نشان کردند. آنها با استفاده از يک معيار بسيار دقيق درجه بندي، رنگ پذيري قوي AMACR را در ٨٨% سرطانهاي پروستات نشان دادند.١١ مطالعه آنها همچنين گوياي رنگ پذيري اکثريت موارد HGPIN با AMACR بود. آنها توصيه کردند جهت افتراق HGPIN از سرطان پروستات از کوکتل آنتي بادي AMACR و مارکر بازال P٦٣ استفاده شود چرا که در HGPIN رنگ پذيري متغير و نقطه اي سيتوپلاسمي AMACR در همراهي با رنگ پذيري قوي و يکنواخت هسته سلولهاي بازال مشاهده مي گردد.١١ طبق مشاهدات ما حساسيت کلي PS٥٠٤ براي کشف سرطان قطعي پروستات ٩٠% بود. دو مورد از هشت سرطان پروستات با سلولهاي کف آلود و دو نمونه از ١٢ کانون کوچک سرطاني فاقد رنگ پذيري بودند که در همگي در اين موارد منفي بودن مارکرهاي سلول بازال بنفع تشخيص سرطان بود. همچنانکه Beach و همکارانش ١٤ در ٤٠% موارد مشاهده کردند بروز PS٥٠٤ در ١٠ مورد از ٤٠ مورد سرطان پروستات ما (٢٥%) به صورت کانوني بود.