بخشی از پاورپوینت
اسلاید 1 :
پرتو كاتدي ،پرتو مثبت ، تابشهاي الكترومغناطيسي ، نظريه هاي كوانتومي ، طيف گسيلي(نشري) هيدروژن،
مدل اتمي بور ، ماهيت دوگانه الكترون ، معادلعه شرودينگر ، اعداد كوانتومي.
جدول تناوبي ، الكترون خواهي، الكترونگاتيوي، بار الكترون ، ساختار اتم ، ايزوتوپ و ايزوبار.
اسلاید 2 :
تاريخچه اتم
- توجه به ايده اتم و پيدايش آن
-
- ايده اوليه يونانيان قديم(B.C 400)
- كوچكترين جزء هر عنصر كه تمام ويژگيهاي آن را داراست.
-
اسلاید 3 :
- تمامي اجسام از چهار عنصر ساخته شده اند
-آتش- گرمي
-هوا– سبكي
- خاك- سردي
- آب- رطوبت
-با آميختن اين عناصر به نسبتهاي گوناگون ، تمامي
اجسام حاصل مي شوند.
اسلاید 4 :
١)ماده از ذره هاي تجزيه نا پذيري به نام اتم ساخته شده است
٢) همه ي اتم هاي يك عنصر مشابه يكديگرند.
٣ )اتم ها نه به وجود مي آيند و نه از بين مي روند.
٤)همه ي اتم هاي يك عنصر جرم يكسان و خواص شيميايي مشابه اي دارند.
٥)اتم ها به هم متصل مي شوند و مولكول ها را به وجود مي آورند.
٦) در هر مولكول همواره نوع و تعداد نسبي اتم هاي سازنده ي آن يكسان است.
7) واكنش هاي شيميايي شامل جابه جايي اتم ها يا تغييردر شيوه ي اتصال آن ها در مولكول ها است. در اين واكنش ها اتم ها خود تغييري نمي كنند.
اسلاید 5 :
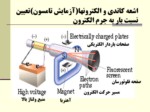
آزمايشهاي لوله اشعه كاتدي را اصلاح و نسبت بار به جرم اين ذرات (الكترونها) را با قرار دادن و انحراف آنها در ميدانهاي الكتريكي و مغناطيسي تعيين نمود.
evH= eE → v = E/H
F = evH = mv2/r →r = mv/eH
e/m = E/rH2
اسلاید 6 :
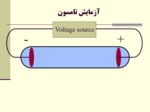
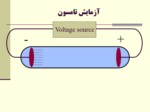
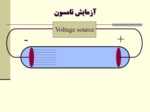
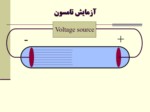
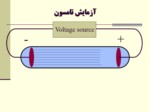
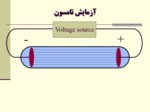
با طراحي لوله كاتدي و انجام آزمايشات تامسون وجود ذرات ريز اتمي اثبات گرديد.
اگر لوله كاتدي به اندازه كافي تخليه گردد، جريان الكتريسيته از طرف كاتد به طرف آند بصورت جرياني از الكترونها بر قرار مي شود.
جريان حاصل از كاتد ،هم توسط ميدان الكتريكي و هم توسط ميدان مغناطيسي منحرف مي شود.
اسلاید 7 :
براساس اين ويژگيها تامسون نشان داد كه اشعه كاتدي جرياني از ذرات باردار منفي است و او اين ذرات را الكترون ناميد.
تامسون توانست نسبت بار به جرم الكترون را به دست آورد.
m/e = 5/69* 10 -9 g/coul
نسبت m/e مستقل از نوع گاز داخل لوله بوده و ثابت است، اين واقعيت نشان مي دهد كه الكترون يك ذره بنيادي و مشترك درتمام اتمهاست.
اسلاید 8 :
رادفور در سال 1920 پیشنهاد کرد که برای توزیع جرم کل اتم باید ذره بدون بار الکتریکی در هسته وجود داشته باشد.شناسایی نوترون به دلیل اینکه بار الکتریکی نداشت و نیزبدست آوردن پارمترهای آن بسیار مشکل بود.در سال 1932 جیمز چادویک وجود این ذرات را اثبات کرد و آن را نوترون(به معنی خنثی) نامید.او همچنین جرم نوترون را براساس بعضی از واکنش های هسته ای که مولد نوترون هستند بدست آورد و برابر 24-10 1/6749* است.
اسلاید 9 :
– A عدد جرمي
– Z عدد اتمي
تعداد پروتونها Z =
تعداد پروتونها+ تعداد نوترونهاA =
در يك اتم خنثي تعداد پروتونها برابر تعداد الكترونهاست.
اسلاید 10 :
بمباران قطعه كوچك و نازكي از طلا با باريكه اي از ذرات آلفا.
نشان دادن ميزان پراكندگي ذرات توسط صفحه فلوئورسان سولفيد روي.
اغلب ذرات آلفا ،بدون تغيير و پراكنده شدن ،از صفحه نازك طلا عبور كرده و فقط تعداد كمي با انحراف زياد از هسته عبور كرده يا بطور كامل مي گردند.