بخشی از پاورپوینت
اسلاید 1 :
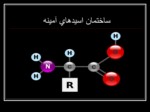
اسيدهاي آمينه
nتعريف اسيدهاي آمينه : اسيدهاي آمينه تركيبات آلي هستندكه در ساختمان آنها دست كم يك گروه آمين و يك گروه كربوكسيل يافت مي شود .
nدر طبيعت 300 نوع اسيد آمينه وجود دارد . اسيدهاي آمينه اي كه در ساختمان پروتئين ها شركت مي كنند ، همگي آلفا آمين و نوع L هستند ( كربني كه به آن گروه كربوكسيل متصل است ، كربن آلفا ناميده مي شود به استثناي اسيد آمينه گليسين در تمام اسيدهاي آمينه آلفا آمين ، اين كربن نا متقارن است ) .
n اسيدهاي آمينه بتا آلانين ( كوآنزيم A ) و گاما آمينوبوتيريك اسيد ( نوروترانسميتر) كه گروه آمين آنها بر روي بتا و گاما قرار گرفته است .
اسلاید 2 :
يونيزاسيون
nگروه كربوكسيل ( COOH ) و آمين ( NH2 ) گروههايي هستند كه مي توانند بر حسب pH محيط تفكيك شوند . گروه كربوكسيل بين دو شكل COOH و COO- وگروه آمين بين دو شكل NH3+ و NH2 بر حسب pH محيط ميتوانند وجود داشته باشند .
n pH ايزوالكتريك به pH اي گفته مي شود كه در آن جمع جبري بارهاي مثبت ومنفي اسيدآمينه برابر باشد .
اسلاید 3 :
براي به دست آوردن pH ايزوالكتريك اسيدآمينه از سه فرمول زير استفاده مي شود :
nبراي اسيدهاي آمينه خنثي :
PK1 اسيدي +PK2 بازي تقسيم بر 2 مي باشد .
nبراي اسيدآمينه هاي اسيدي :
PK1 اسيدي +3PK اسيدي تقسيم بر 2 مي باشد .
nبراي اسيدآمينه هاي بازي :
2 PK بازي +PK3 بازي تقسيم بر 2 مي باشد .
اسلاید 4 :
حركت به طرف قطبها
n همه اسيدهاي آمينه وپروتئين ها در بالاي pH ايزوالكتريك خود داراي بار منفي ، به سمت قطب مثبت حركت مي كنند و در پايين pH ايزوالكتريك خود ( pH اسيدي ) داراي بار مثبت هستند ، كه به سمت قطب منفي حركت مي كنند.
nاسيدهاي آمينه اسيدي در pH فيزيولوژيك داراي بار منفي و اسيدهاي آمينه بازي داراي بارمثبت هستند .
nاسيد آمينه هيستيدين مهم ترين اهميت را در خاصيت بافري پروتئينها ايفا مي كند .
اسلاید 5 :
انواع طبقه بندي اسيدهاي آمينه
.1طبقه بندي بر اساس ماهيت R ( قطبي وغير قطبي )
.2طبقه بندي بر اساس ضروري يا غيرضروري
اسلاید 6 :
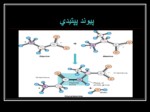
ساختمان پپتيدها و پروتئينها
nتعريف : در اثر اتصال دويا چند اسيد آمينه به يكديگر پپتيدها به وجود مي آيند . پيوندي كه باعث اين اتصال مي شود ، پيوند پپتيدي نام دارد كه در اثر تركيب گروه آمين و گروه كربوكسيل آلفاي اسيدهاي آمينه با هم به وجود مي آيد .
n برحسب تعريف ، بر اثراتصال 5،4،3،2و... دي ،تري ، تترا ، پنتا ، ... پپتيد به وجود مي آيد كه اوليگوپپتيد ناميده مي شوند .
n به طور كلي اگر تعداد اسيدهاي آمينه موجود در پپتيد بيش از 50 عدد باشد يا به عبارت ديگر از 50000 دالتون بيشتر باشد ، زنجير را پلي پپتيد يا پروتئين مي نامند .
اسلاید 7 :
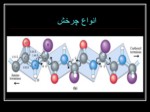
ساختمانهاي مختلف پروتئينها
.1ساختمان اول
همان گونه كه گفته شد ، اسكلت پلي پپتيدها به صورت زيگزاگي وكشيده است . اين شكل را اصطلاحاً ساختمان اول پروتئين گويند ، كه در آن توالي اسيدهاي آمينه ، نوع پلي پپتيد را تعيين مي كند .
nپيوندهاي كوالانسي ( پپتيدي ) باعث ايجاد اين ساختمان مي شوند .
اسلاید 8 :
ساختمان دوم
nدر اثر حركت اسكلت پلي پپتيدي درفضا دو شكل منظم مارپيچ آلفا ويا صفحات چين داربتا به وجود مي آيد كه ساختمان دوم خوانده مي شود.
nنوع اسيدهاي آمينه موجود در يك قطعه پلي پپتيدي تعيين كننده ساختمان دوم آن است .
nدر ساختمان دوم علاوه بر پيوند هيدروژني انواع ديگر پيوندها يعني كوالانسي ( دي سلفيد )، نمكي ( بين اسيدهاي آمينه اسيدي وبازي ) ،هيدروفوبي ( بين اسيدهاي آمينه غير قطبي ) تشكيل مي شود .
اسلاید 9 :
ساختمان سوم
nدر اثر تا شدن زنجيره پلي پپتيدي بر روي خود ، اسيدهاي آمينه اي كه در فواصل نسبتاً دور از هم قرارگرفته اند نيز در كنار هم قرار مي گيرند .
nدر اين ساختمان نيز انواع پيوندهاي قوي و ضعيف تشكيل مي شوند ، پلي پپتيد هايي كه تنها از يك زنجيره تشكيل شده اند ، حداكثر به ساختمان سوم مي رسند .
اسلاید 10 :
ساختمان چهارم
nدراثركنار هم قرار گرفتن حداقل دوپلي پپتيد كه به ساختمان سوم رسيده اند ، ساختماني ايجاد مي شود كه ساختمان چهارم خوانده مي شود . دراين ساختمان نيز انواع پيوندهاي قوي وضعيف تشكيل مي شوند . اين ساختمان منحصراً در پروتئين هاي اوليگومر ( بيش از يك زير واحد دارند ) يافت مي شود .